Kiyokawa, Kensuke
- 位置選択性にも注目。 -
(April 19, 2023)
読みたい論文シリーズ− 2023年2Q
読みたいけと読んでいない論文を、構造式を描きながら紹介します。読んでないので時々間違えます(2023年4〜6月)。
読みたいけと読んでいない論文を、構造式を描きながら紹介します。読んでないので時々間違えます(2023年4〜6月)。
Keywords: BrCN; TFPB; carbon–carbon bond formation; umpolung; Kiyokawa, Kensuke; Minakata, Satoshi
Tris(pentafluorophenyl)borane-Catalyzed Stereospecific Bromocyanation of Styrene Derivatives with Cyanogen Bromide (Kiyokawa, Kensuke; Noguchi, Ikumi; Nagata, Takaya; Minakata, Satoshi)Org. Lett. 2023, 25 (14), 2537–2542.
URL (Doi): 10.1021/acs.orglett.3c00727
 |
March 14, 2023[読みたい論文] スルホン酸シアニドを使ってアルケンのオキシシアノ化
そのジアステレオ選択性はどこから。
Angew. Chem. Int. Ed. 2023, 62 (12), e202218743.
そのジアステレオ選択性はどこから。
Angew. Chem. Int. Ed. 2023, 62 (12), e202218743.
スチレン化合物と臭化シアンの反応。ペンタフルオロフェニル基が3つ結合したホウ素化合物がルイス酸触媒として機能します。
反応の特徴のひとつが立体選択性。攻撃面が特異的。アルケンへの求電子付加といえば教科書的にはanti–付加ですが、この論文の反応ではsyn–付加、つまりブロモ基とシアノ基がアルケンの同じ面側からくっつくのだとか。それを可能にするのが臭化シアンのホウ素ルイス酸への配位なのでしょうが、付加反応にどう関わるのかは、本文を読まないと細かいところがわからなさそう。
Supporting Informationにはその臭化シアン-ホウ素ルイス酸錯体(複合体かも)のものと思われるスペクトルが数種類あって、赤外吸収のものについては臭化シアンの炭素-窒素三重結合由来の吸収がホウ素ルイス酸への配位によって高波数側へシフトする模様。13C NMRスペクトルの臭化シアンのピークも低磁場側へシフトしていて、両スペクトルから臭化シアンの炭素が…
 |
そう考えると反応の「位置」選択性、スチレン化合物の末端側にシアノ基が結合、ベンジル炭素側にブロモ基が結合した化合物が生成するのも矛盾しないんですよね。
その辺りどうなっているのか知りたいので、読みたい論文に追加しました。もちろんsyn–付加のメカニズムも。

[読みたい論文] スルホン酸シアニドを使ってアルケンのオキシシアノ化
そのジアステレオ選択性はどこから。
Angew. Chem. Int. Ed. 2023, 62 (12), e202218743.
そのジアステレオ選択性はどこから。
Angew. Chem. Int. Ed. 2023, 62 (12), e202218743.
最近の記事
July 14, 2025
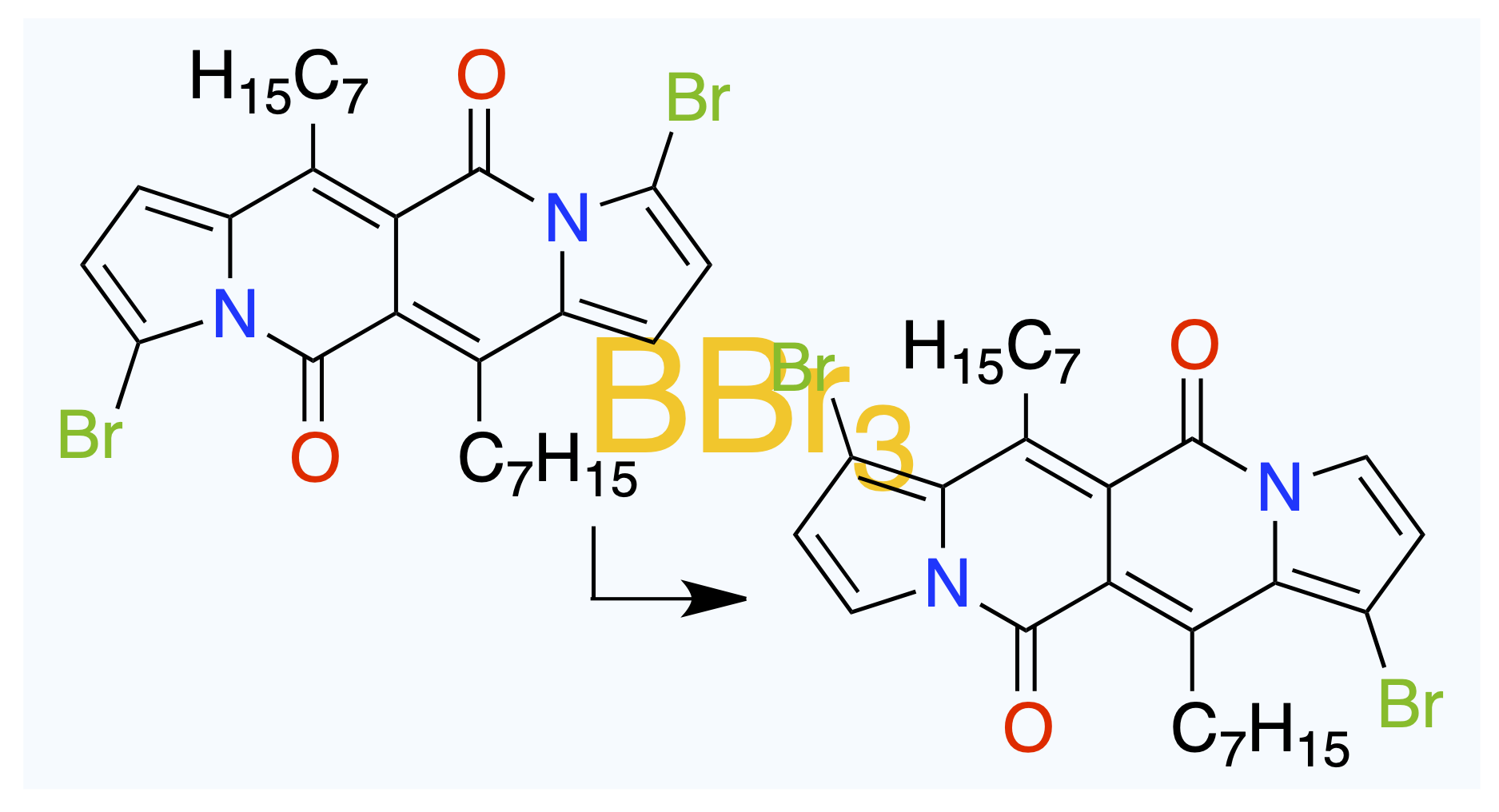
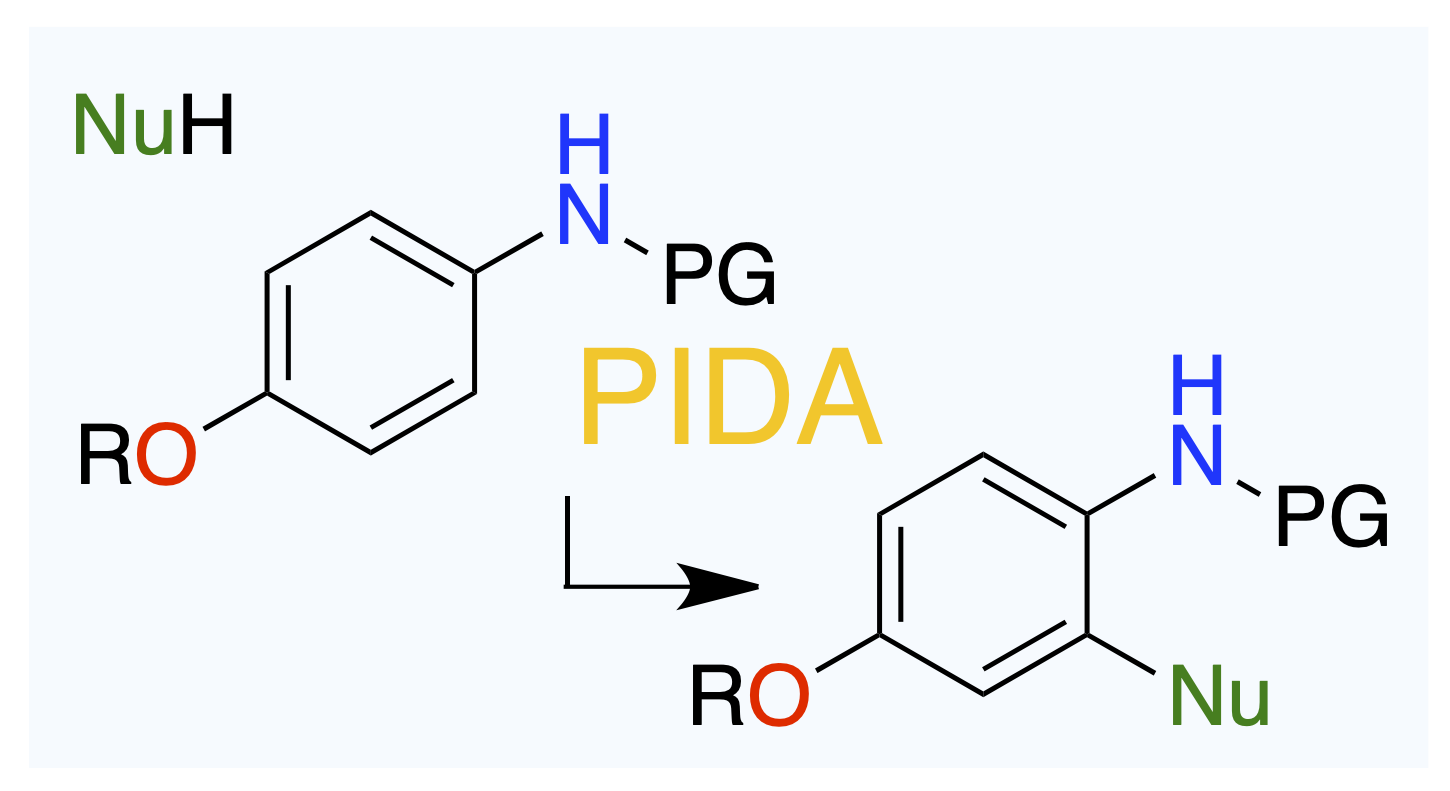
親電子置換もいける。
Org. Lett. 2025, 27 (25), 6566–6570.
Org. Lett. 2025, 27 (25), 6566–6570.
July 11, 2025
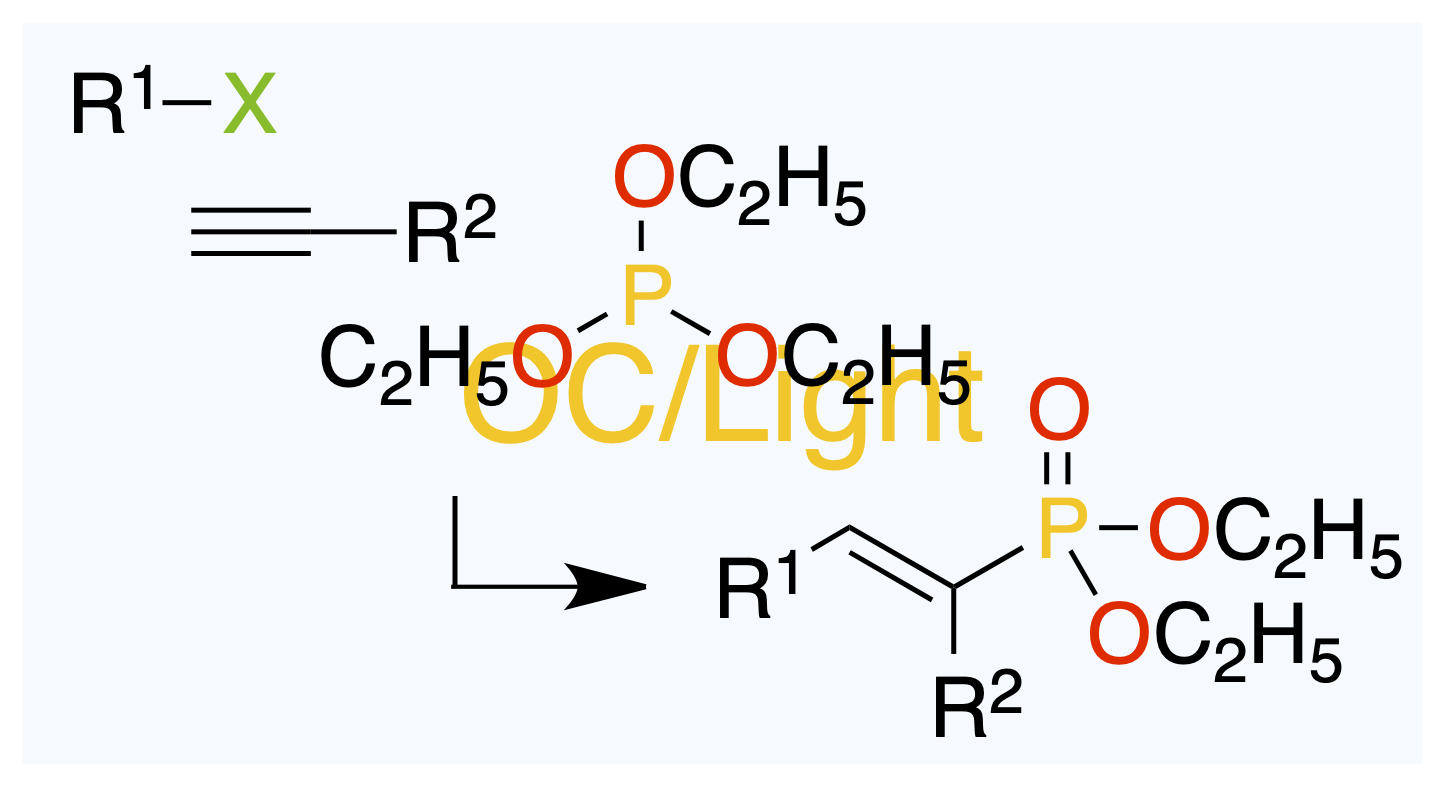
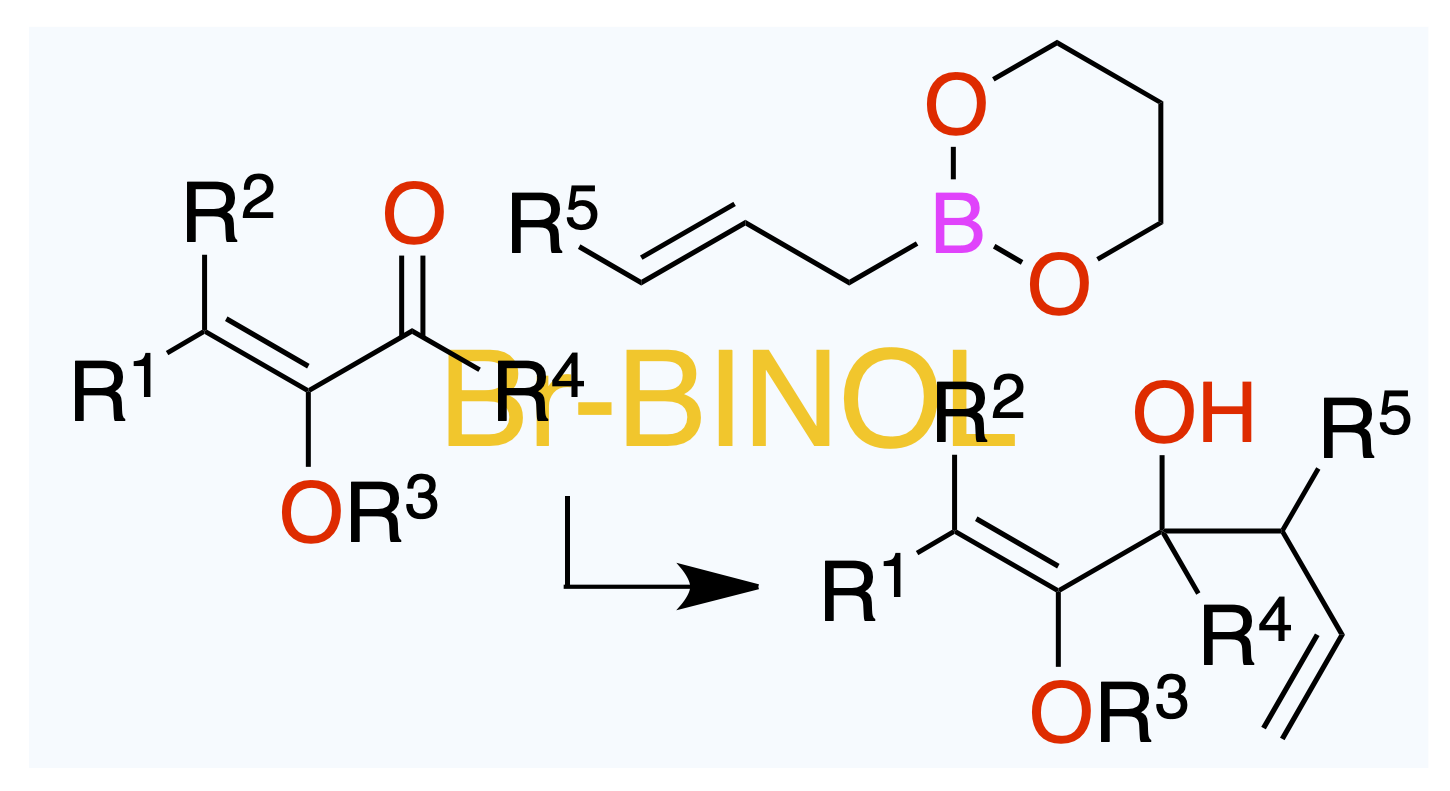
1,2–付加でのアリルアルコール経由で。
Org. Lett. 2025, 27 (25), 6557–6560.
Org. Lett. 2025, 27 (25), 6557–6560.
July 9, 2025
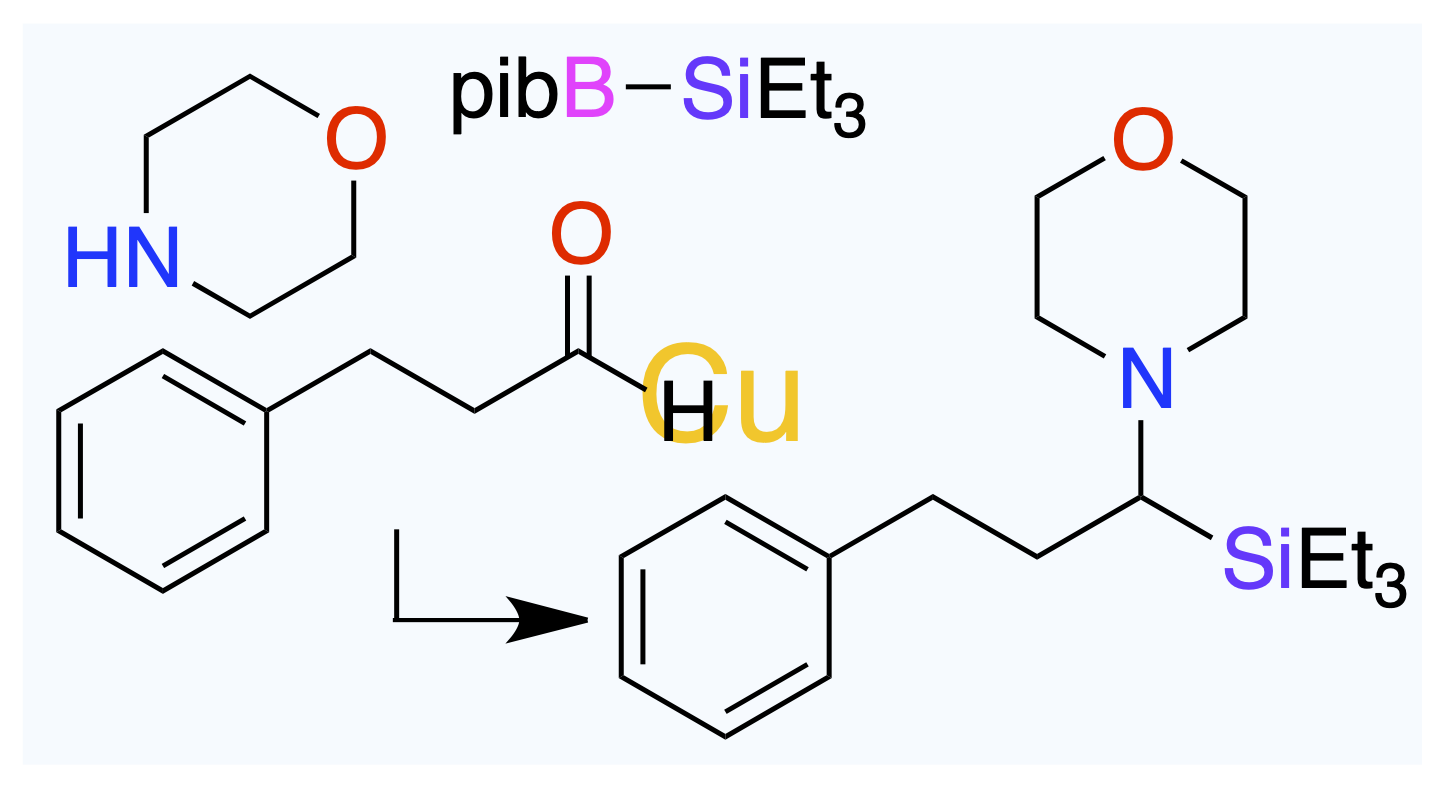
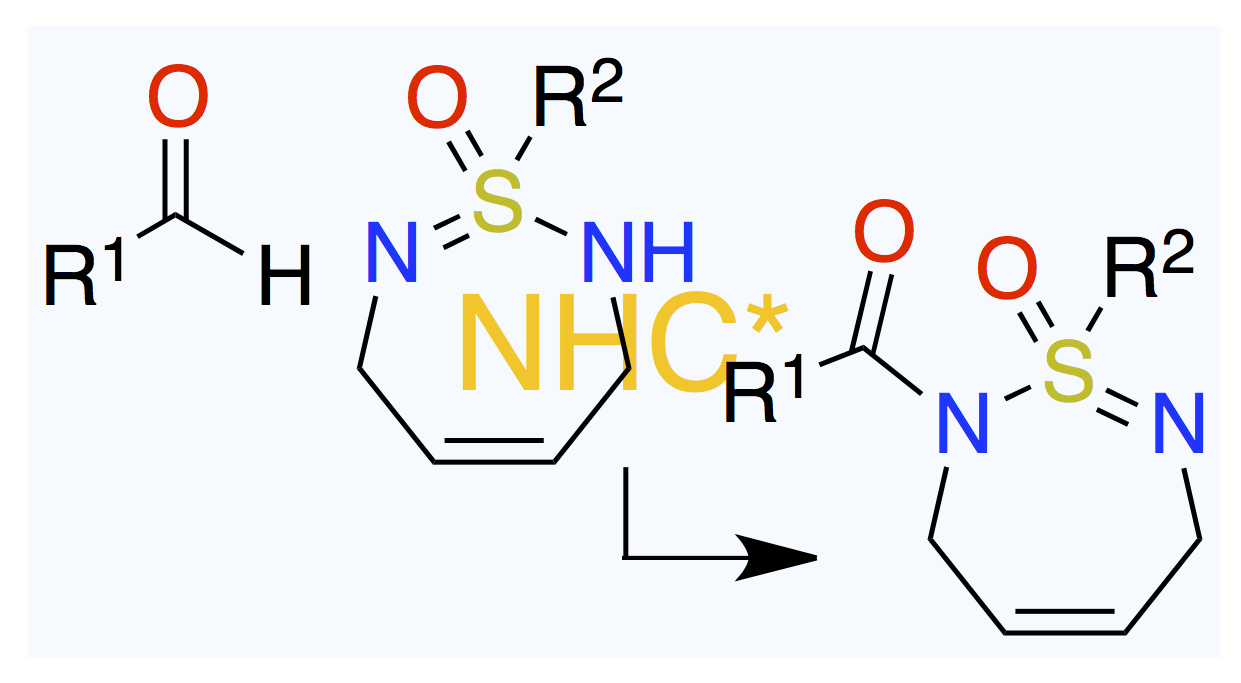
元の化合物はキラルかアキラルか。
Angew. Chem. Int. Ed. 2025, 64 (27), e202506929.
Angew. Chem. Int. Ed. 2025, 64 (27), e202506929.
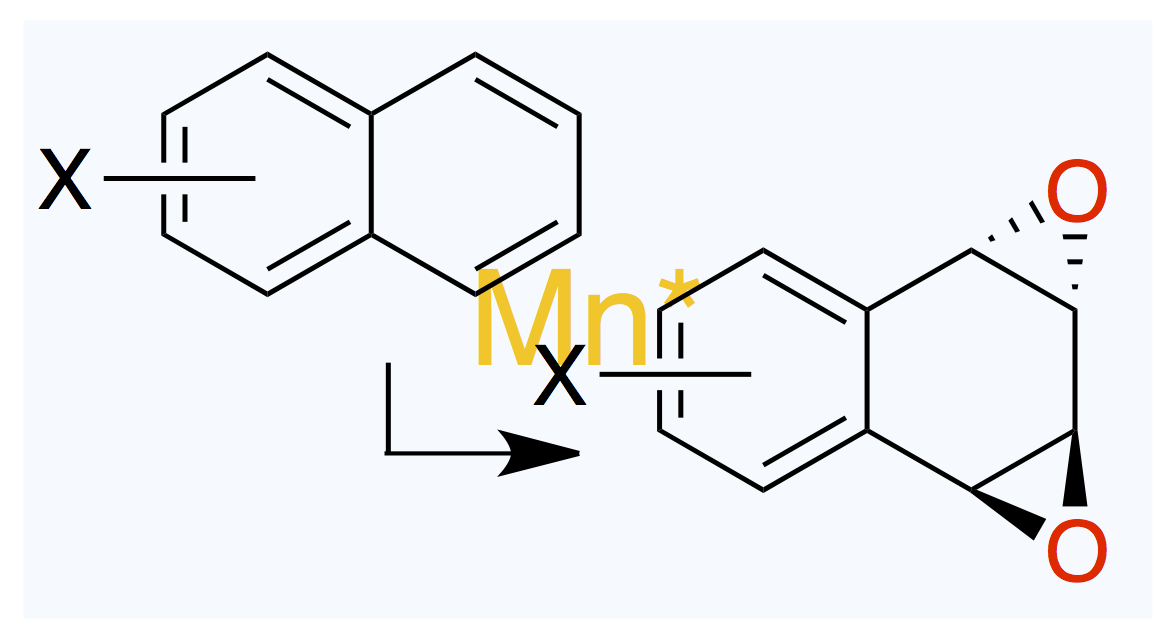
最近よく読まれています
定番の記事








(c) Nanoniele, 2003-
The domain name we own is "nanoniele.jp". We have nothing to do with other domains containing "nanoniele", except "nanoniele.blogspot".
The domain name we own is "nanoniele.jp". We have nothing to do with other domains containing "nanoniele", except "nanoniele.blogspot".